23家企業生產的25批(臺)醫療器械不合格 歐姆龍電子血壓計再上榜
中國食品藥品網訊(記者 李碩) 5月5日,國家藥監局發布《關于發布國家醫療器械監督抽檢結果的通告》。通告顯示,國家藥監局對電子血壓計、一次性使用醫用口罩、醫用X射線防護用具(防護衣、裙、圍脖等)、人體血液及血液成分袋式塑料容器(血袋)等7個品種共151批(臺)的產品進行質量監督抽檢,歐姆龍(大連)有限公司等23家企業生產的25批(臺)產品不符合標準規定。
被抽檢項目為標識標簽、說明書等項目不符合標準規定的醫療器械產品,涉及7家企業的2個品種7批(臺)。
7批(臺)抽檢(標識標簽說明書等項目)不合格產品名單
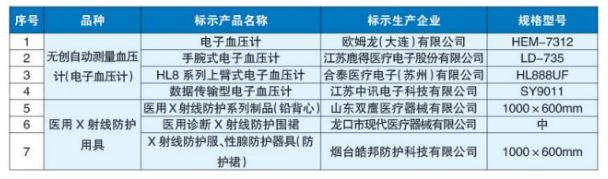
一是無創自動測量血壓計(電子血壓計)4家企業4臺產品不符合標準規定。其中,作為知名跨國企業,標示為歐姆龍(大連)有限公司生產的1臺電子血壓計(型號HEM-7312,批號201801L,出廠編號20180103173LG)標識不合格,這是繼今年2月份抽檢被發現其生產的1臺電子血壓計(型號HEM-8611,批號201804L,出廠編號20180407322LF)存在“泄氣”和“標識不合格”問題以來,該公司第二次被列入國家藥監局醫療器械抽檢不合格名單。另外,標示為江蘇鹿得醫療電子股份有限公司生產的1臺手腕式電子血壓計、合泰醫療電子(蘇州)有限公司生產的1臺HL8系列上臂式電子血壓計、江蘇中訊電子科技有限公司生產的1臺數據傳輸型電子血壓計,標識要求也不符合標準規定。
二是醫用X射線防護用具(防護衣、裙、圍脖等)3家企業3批次產品標記不符合標準規定。它們是標示為山東雙鷹醫療器械有限公司生產的1批次醫用X射線防護系列制品(鉛背心)、龍口市現代醫療器械有限公司生產的1批次醫用診斷X射線防護圍裙、煙臺皓邦防護科技有限公司生產的1批次X射線防護服、性腺防護器具(防護裙)。
被抽檢項目不符合標準規定的醫療器械產品,涉及17家企業的6個品種19批(臺)。
19批(臺)抽檢不符合標準規定產品名單
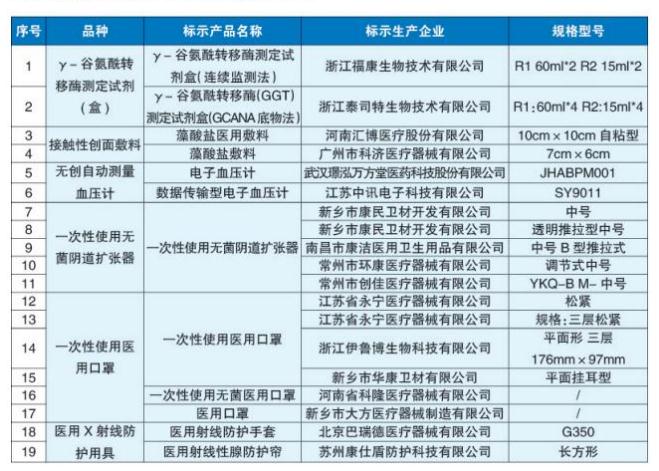
一是γ-谷氨酰基轉移酶測定試劑(盒)2家企業2批次產品。涉及標示為浙江福康生物技術有限公司生產的1批次γ-谷氨酰轉移酶測定試劑盒(連續監測法)、浙江泰司特生物技術有限公司生產的1批次γ-谷氨酰轉移酶(GGT)測定試劑盒(GCANA底物法),線性不符合標準規定。
二是接觸性創面敷料2家企業2批次產品酸堿度試驗不符合標準規定,涉及標示為河南匯博醫療股份有限公司生產的1批次藻酸鹽醫用敷料、廣州市科濟醫療器械有限公司生產的1批次藻酸鹽敷料。
三是無創自動測量血壓計(電子血壓計)2家企業2臺產品。標示為武漢璟泓萬方堂醫藥科技股份有限公司生產的1臺電子血壓計,最大袖帶壓、可重復性、壓力傳感器準確性不符合標準規定;標示為江蘇中訊電子科技有限公司生產的1臺數據傳輸型電子血壓計,指示燈的顏色不符合標準規定。
四是一次性使用無菌陰道擴張器4家企業5批次產品。標示為新鄉市康民衛材開發有限公司生產的2批次、南昌市康潔醫用衛生用品有限公司生產的1批次一次性使用無菌陰道擴張器,環氧乙烷殘留量不符合標準規定;標示為常州市環康醫療器械有限公司生產的1批次一次性使用無菌陰道擴張器,抗變形能力不符合標準規定;標示為常州市創佳醫療器械有限公司生產的1批次一次性使用無菌陰道擴張器,結構強度不符合標準規定。
五是一次性使用醫用口罩5家企業6批次產品。標示為江蘇省永寧醫療器械有限公司生產的2批次一次性使用醫用口罩,口罩帶、細菌過濾效率(BFE)不符合標準規定;標示為浙江伊魯博生物科技有限公司生產的1批次一次性使用醫用口罩、新鄉市華康衛材有限公司生產的1批次一次性使用醫用口罩、河南省科隆醫療器械有限公司生產的1批次一次性使用無菌醫用口罩,細菌過濾效率(BFE)不符合標準規定;標示為新鄉市大方醫療器械制造有限公司生產的1批次醫用口罩,微生物指標不符合標準規定。
六是醫用X射線防護用具(防護衣、裙、圍脖等)2家企業2批次產品。標示為北京巴瑞德醫療器械有限公司生產的1批次醫用射線防護手套,材料不符合標準規定;標示為蘇州康仕盾防護科技有限公司生產的1批次醫用射線性腺防護簾,設計不符合標準規定。
《中國醫藥報》社版權所有,未經許可不得轉載使用。

















