每周醫藥看點(2月23日—3月1日)
- 2026-03-05 15:37
- 作者:
- 來源:中國醫藥報
罕見病藥物研發交流座談會在國家藥監局藥品審評中心(CDE)召開;CDE就罕見疾病創新藥物研發鼓勵試點計劃(“關愛計劃-延伸”)相關工作文件公開征求意見……2月23日—3月1日,醫藥行業的這些動態值得關注。
行業政策及藥監動態
1.罕見病藥物研發交流座談會在CDE召開。會議指出,國家藥監局不斷加強罕見病用藥保障,打好政策“組合拳”,建立并暢通鼓勵創新、加快引進和臨時進口“三條通道”,我國罕見病用藥的上市數量和速度均顯著提升,僅2025年就有48個罕見病藥物獲批上市。
2.CDE就罕見疾病創新藥物研發鼓勵試點計劃(“關愛計劃-延伸”)相關工作文件公開征求意見。制定該試點計劃,旨在鼓勵創新藥向臨床治療需求迫切的罕見疾病領域布局,關注并探討解決源頭性創新研發中的科學問題。
3.CDE發布《新藥全球同步研發中基于多區域臨床試驗數據進行獲益-風險評估的指導原則(試行)》。指導原則主要闡述在新藥全球同步研發中基于多區域臨床試驗數據進行上市申請時,對單區域進行獲益-風險評估的一般要求,重點關注在獲益-風險評估框架下對全球同步研發臨床試驗數據的評估考慮。
4.CDE發布《化學合成寡核苷酸藥物(創新藥)藥學研究技術指導原則(試行)》。指導原則適用于反義寡核苷酸,小干擾核酸(siRNA)、核酸適配體等化學合成寡核苷酸創新藥物的上市申請,不包括mRNA等生物合成的核酸藥物、抗體偶聯核酸藥物等。
5.國家藥監局食品藥品審核查驗中心就《藥品生產企業整改報告編訂指南(征求意見稿)》公開征求意見。征求意見稿中所指的整改報告是指藥品生產企業接受藥品監管部門組織的現場檢查后,針對檢查發現的缺陷,按照實際整改情況,編訂的反映企業調查分析、風險評估、風險控制(含糾正措施和預防措施)、完成情況等內容以及整改證明材料的一系列文件和記錄。
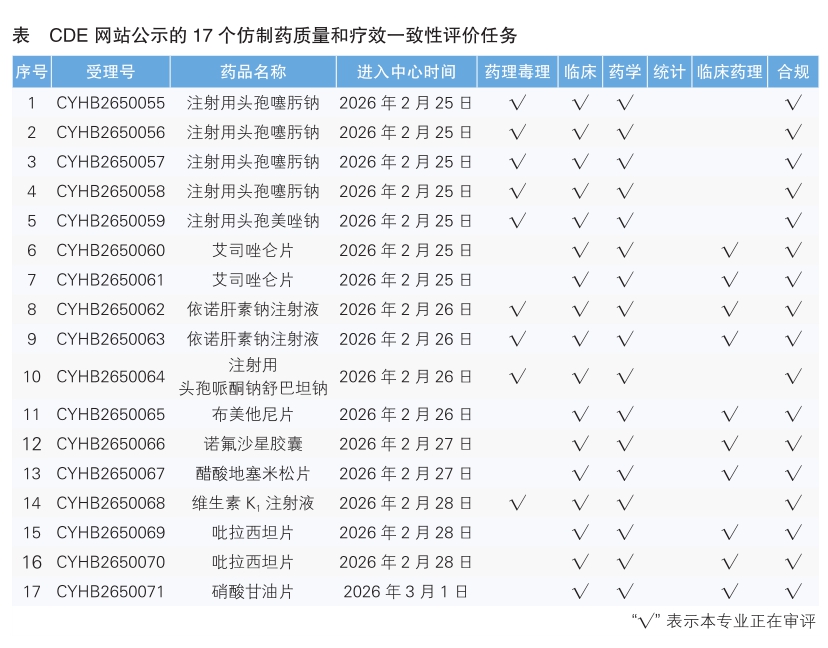
6.CDE網站公示17個仿制藥質量和療效一致性評價任務(詳見表),涉及注射用頭孢噻肟鈉等品種。
產品研發上市信息
1.國家藥監局發布5期藥品批準證明文件送達信息,共包括268個受理號,涉及山東益健藥業有限公司等企業。
2.CDE承辦受理112個新藥上市申請,包括溫膽湯顆粒等。
3.亞虹醫藥發布公告稱,公司產品APL-1702擬用于治療宮頸高級別鱗狀上皮內病變患者的上市許可申請已獲得歐洲藥品管理局受理。
4.匯宇制藥宣布,公司向美國食品藥品管理局(FDA)申報的依托泊苷注射液、氟尿嘧啶注射液的新藥申請(NDA)均已獲得批準。
醫藥企業觀察
1.前沿生物宣布,與葛蘭素史克達成獨家授權許可協議。根據協議,葛蘭素史克將獲得前沿生物兩款siRNA管線在全球范圍內的獨家開發、生產及商業化權利;前沿生物將獲得4000萬美元首付款,并在兩個項目中累計獲得最高9.63億美元的開發、監管及商業化里程碑付款,同時享有兩款產品全球凈銷售額的分級特許權使用費。
2.和鉑醫藥宣布,與英國Solstice Oncology公司達成授權協議及股權合作,授予對方一款臨床階段候選產品HBM4003在大中華區以外地區的獨家開發及商業化權益。根據協議,和鉑醫藥將獲得總價值逾1.05億美元的前期對價。此外,基于未來特定里程碑事件的達成,和鉑醫藥還有資格獲得最高約11億美元的開發、監管及商業化里程碑付款,以及基于大中華區以外地區凈銷售額的分級特許權使用費。
3.先為達生物宣布,與輝瑞中國就埃諾格魯肽注射液達成商業化戰略合作協議。根據協議,輝瑞中國將獲得埃諾格魯肽注射液在許可區域的獨家商業化權益;先為達生物有權獲得輝瑞中國支付的最高可達4.95億美元的首付款、注冊及銷售里程碑付款。
4.藥明合聯宣布,與美國生物科技公司Earendil Labs達成戰略合作。根據合作協議,藥明合聯將向Earendil Labs授權其自主研發的WuXiTecan-2載荷連接子技術,并授予Earendil Labs在全球范圍內針對多個特定靶點抗體偶聯候選藥物的獨家開發權。本次合作潛在總交易金額預計可達8.85億美元。
藥品集中采購
1.國家組織集采藥品協議期滿品種接續采購辦公室發布《關于公布國家組織集采藥品協議期滿品種接續采購(LC-YPJX-2026-1)中選結果的通知》。根據通知,浙江海正藥業股份有限公司的阿他伐他汀口服常釋劑型等中選。
2.上海市醫藥集中招標采購事務管理所發布《關于暫停部分藥品采購資格的通知》。通知顯示,根據《國家藥監局關于27批次不符合規定藥品的通告(2026年第5號)》,自2月28日0時起,暫停唐山紅星藥業有限責任公司兩款不同規格的醋酸曲安奈德乳膏采購資格。(劉鶴整理)
《中國醫藥報》社版權所有,未經許可不得轉載使用。
(責任編輯:劉思慧)
右鍵點擊另存二維碼!
-
相關閱讀
-
為你推薦