2月份美國Clinicaltrial數據庫臨床試驗數據顯示—— 糖尿病、乳腺癌、肥胖等適應證成研發熱點
- 2026-04-09 13:33
- 作者:陳宇哲
- 來源:中國醫藥報
根據美國Clinicaltrial數據庫數據,今年2月份,全球新開由企業資本主導的臨床試驗總數為707項,數量較1月份下降5.23%;單月新開臨床試驗數量高于去年同期水平,同比上升16.67%。
熱門領域分布
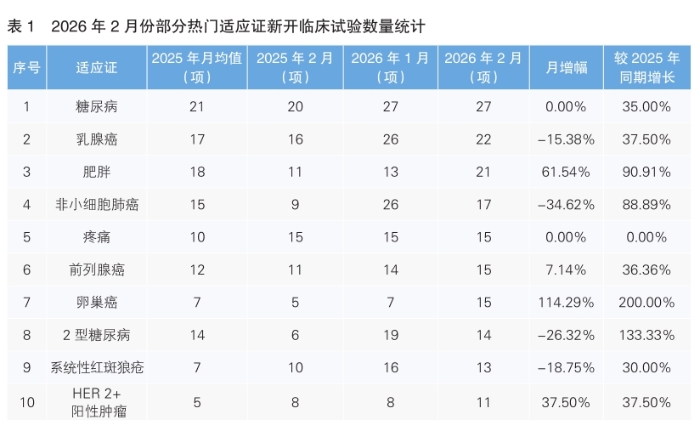
從2月份新開臨床試驗熱門適應證來看,糖尿病為最熱門的研發領域,新開臨床試驗27項,環比持平,同比上漲35%。2月份新開臨床試驗數量上升幅度最大的熱門適應證為卵巢癌,新開臨床試驗15項,環比上升114.29%,同比上升200.00%;新開臨床試驗數量下降幅度最大的熱門適應證為非小細胞肺癌,由1月份的26項下降到17項,下降幅度為34.62%,但比去年同期上升88.89%。(詳見表1)
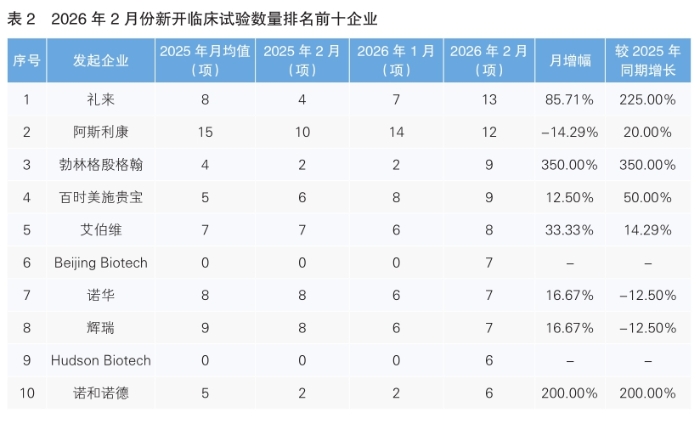
對新開臨床試驗的發起單位進行統計后發現,2月份發起臨床試驗最多的企業是禮來,新開臨床試驗13項,環比上升85.71%,同比上漲225%。其次為阿斯利康,新開臨床試驗12項,環比下降14.29%,同比增長20%。新開臨床試驗數量上升幅度最大的企業為勃林格殷格翰,新開臨床試驗9項,環比同比均增長350%。(詳見表2)
對臨床試驗的申請國家和地區進行統計后發現,2月份美國仍為臨床試驗開展最為主要的國家,新開臨床試驗264項;其次是中國,新開臨床試驗91項。2月份新開臨床試驗數量增長幅度最大的是西班牙,由1月份的17項增長為22項,增長幅度為29.41%。
頭部企業表現
禮來2月份新開的13項臨床試驗中,有6項為Ⅲ期臨床試驗。其中,有4項試驗藥物為Eloralintide,2項試驗藥物為Brenipatide。Eloralintide是禮來研發的全球首款高選擇性長效胰淀素1受體(AMY1R)激動劑,可精準模擬天然胰淀素,通過中樞神經系統、外周組織器官雙重通路調控體重。其對AMY1R的親和力為降鈣素受體的12倍,能顯著減少惡心、嘔吐等胃腸道不良反應,耐受性優于非選擇性同類藥物。該藥4項Ⅲ期臨床試驗的適應證分別為肥胖(NCT07392190)、2型糖尿病合并肥胖(NCT07321886)、阻塞性睡眠呼吸暫停(NCT07369011)、骨關節炎(NCT07353931)。Brenipatide是禮來繼替爾泊肽之后布局的第二款長效GLP-1R/GIPR雙靶點激動劑,但二者產品定位差異化顯著,Brenipatide主要聚焦神經精神疾病領域,涵蓋成癮、抑郁、雙相情感障礙等。該藥物保留了GLPR-1/GIPR雙重激動活性,經結構優化,提升中樞穿透性與神經調控能力。此次2項Ⅲ期臨床試驗分別針對重度抑郁障礙(NCT07412756)和1型糖尿病(NCT07222332)。
阿斯利康2月份新開的12項臨床試驗中,包含2項Ⅲ期臨床試驗,試驗藥物均為生物藥。其中1項試驗藥物為Sonesitatug vedotin,適應證為胃癌(NCT07431281)。該藥是一款靶向CLDN18.2的抗體偶聯藥物(ADC),由我國藥企康諾亞生物研發,阿斯利康負責全球開發。另1項試驗藥物為AZD0120,適應證為復發難治性多發性骨髓瘤(NCT07391657)。該藥是一款BCMA/CD19雙靶向自體CAR-T細胞療法。
勃林格殷格翰2月份新開的9項臨床試驗中,包含3項Ⅲ期臨床試驗,試驗藥物分別為Tenecteplase、BI 764198、Nerandomilast,適應證分別為急性缺血性腦卒中(NCT07361302)、局灶節段性腎小球硬化(NCT07220083)、家族性肺纖維化(NCT07201922)。其中,Tenecteplase為重組組織型纖溶酶原激活劑,屬靜脈溶栓藥物,主要用于急性心肌梗死、急性缺血性腦卒中的溶栓治療。BI 764198是勃林格殷格翰研發的First-in-Class口服選擇性TRPC6抑制劑,能夠特異性阻斷TRPC6通道,以減少鈣內流,保護足細胞,并通過修復腎小球濾過屏障顯著降低蛋白尿。Nerandomilast是勃林格殷格翰研發的全球首款高選擇性口服磷酸二酯酶4B(PDE4B)抑制劑,主要用于特發性肺纖維化及進展性肺纖維化的治療。
百時美施貴寶2月份新開的9項臨床試驗中,有2項為Ⅲ期臨床試驗,試驗藥物均為Xanomeline-trospium chloride(KarXT),適應證聚焦自閉癥相關易怒障礙,分別針對自閉癥譜系障礙(NCT07285798)與非譜系障礙人群(NCT07325136)。該藥是全球首個非多巴胺機制抗精神分裂癥創新藥,為口服毒蕈堿M1/M4受體偏好性激動復方制劑,通過激活中樞膽堿能M1/M4受體發揮療效。
輝瑞2月份新開的7項臨床試驗中,僅1項推進至Ⅲ期臨床試驗,試驗藥物為PF-08653944(曾用名:MET-097i),適應證為肥胖(NCT07400679)。該藥是輝瑞開發的超長效、完全偏向型GLP-1受體激動劑,具備差異化分子設計,可優先激活減重獲益相關信號通路,降低傳統GLP-1類藥物常見不良反應風險。在劑型開發方面,該藥主打每月1次皮下注射,大幅降低給藥頻次。
諾和諾德2月份新開的6項臨床試驗中,僅有1項Ⅲ期臨床試驗,試驗藥物為NNC0487-0111,適應證為肥胖(NCT07339423)。該藥是諾和諾德自主研發的GLP-1/胰淀素雙受體激動劑,可憑借單一分子同時激活兩條代謝通路,形成協同增效效應。在劑型設計上,該藥同步布局了每周1次皮下注射+口服片劑兩條路線,兼顧依從性與便捷性,主要聚焦肥胖、超重兩大治療賽道。(數據來源于美國Clinicaltrial數據庫,統計時間為2026年3月22日)
《中國醫藥報》社版權所有,未經許可不得轉載使用。
(責任編輯:劉思慧)
右鍵點擊另存二維碼!
-
相關閱讀
-
為你推薦