基因編輯療法研發管線騰飛在即
- 2020-05-28 17:02
- 作者:
- 來源:藥明康德
在過去18個月里,有11項基因編輯研發項目在美國或歐盟進入臨床開發階段,其中6項基于CRISPR-Cas基因編輯系統。現在基因編輯研發管線包括這一技術在體外基因編輯、癌癥免疫學和體內基因編輯方面的應用。近日,NatureReviewsDrugDiscovery上發表的一篇綜述對基因編輯的研發管線進行了深度盤點。

多種基因編輯技術平臺進入臨床開發階段
提到基因編輯技術,人們可能首先想到的是CRISPR-Cas基因編輯系統。這一系統通過使用向導RNA(guideRNA),讓Cas酶能夠識別基因組中的特定序列,從而對DNA或RNA序列進行精準的切割。CRISPR-Cas基因編輯系統因為它的簡便和可編程性,在問世以后就得到了學術界和研發界的廣泛應用。
然而,基因編輯的工具并不只有CRISPR。目前,多項基于其它基因編輯技術平臺的研發項目也已經進行臨床開發階段。其中之一是鋅指核酸酶(Zinc-fingernucleases,ZFNs),這類核酸內切酶并不依靠RNA,而是依靠鋅指蛋白來識別特定DNA序列。Sangamo公司在開發基于鋅指核酸酶的基因編輯系統方面積累了很多經驗。由于需要對鋅指蛋白進行修改來改變ZFN的靶向序列特異性,基于鋅指核酸酶的基因編輯系統沒有CRISPR基因編輯系統那么簡便。然而,ZFN基因編輯系統也有自己的優勢。例如,它并不是源于細菌的蛋白,因此在人體中使用時可能更不容易激發人體的免疫反應。而且,ZFN識別DNA序列的蛋白域與其它基因編輯系統相比更小,更容易裝進遞送基因編輯系統的載體之中。
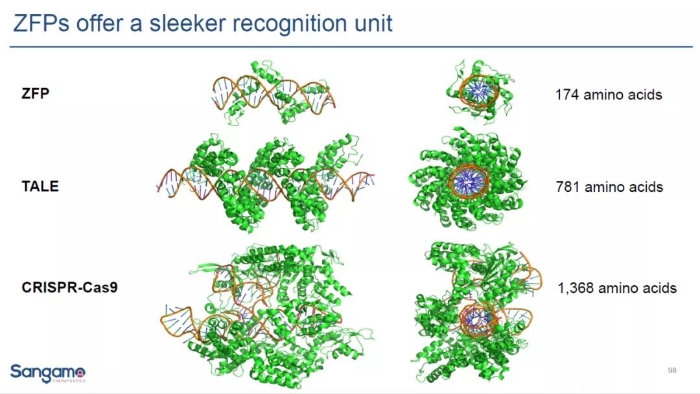
▲不同基因編輯系統核酸序列識別亞基大小
除了CRISPR和鋅指核酸酶以外,其它的基因編輯技術平臺包括TALEN,大范圍核酸酶(meganulease),以及綜合TALEN和大范圍核酸酶構建的megaTAL技術。它們都存在各自的優缺點,也可以在不同的應用場景下發揮作用。
體外基因編輯研發管線
最初的基因編輯研發項目聚焦于在體外對細胞進行編輯。從新技術開發的角度來講這并不意外,在體外對細胞的基因組進行編輯,可以避開困擾基因編輯的多種障礙。以CRISPR為例,基因編輯的一個主要障礙是如何將較大的基因編輯系統遞送到細胞內部,而體外基因編輯可以使用電穿孔技術打開細胞膜這一屏障,讓基因編輯系統比較容易地進入細胞。
CRISPR基因編輯技術需要克服的另外兩個難關是防止基因編輯的“脫靶效應”和Cas蛋白產生的免疫原性。而在體外對細胞進行基因編輯可以繞開人體的免疫應答問題,并且可以對編輯后的細胞進行檢測,發現和清除出現“脫靶效應”的細胞。提高潛在療法的安全性。
目前,體外基因編輯研發項目主要聚集于血紅蛋白疾病和癌癥免疫學兩大領域。無論是血紅蛋白疾病還是血液癌癥,已有的基因療法和細胞療法的成功已經為開發基于基因編輯的創新療法鋪平了道路。同時,它們也代表著患者未被滿足的醫療需求。
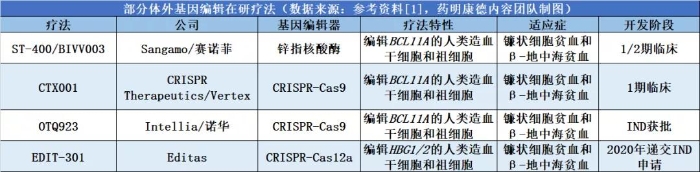
在血紅蛋白疾病方面,數項治療鐮狀細胞貧血(SCD)和β地中海貧血的基因編輯項目已經進入臨床開發階段。其中,Sangamo和賽諾菲聯合開發的ST-400/BIVV003使用ZFN基因編輯系統對從患者體內獲得的造血干細胞和祖細胞(HSPCs)進行基因編輯,通過對BCL11A基因的編輯讓細胞能夠重新表達胎兒血紅蛋白。去年在ASH年會上公布的初步數據表明,接受改造過的HSPCs治療的三名患者中有兩名患者的胎兒血紅蛋白水平顯著提高。
CRISPRTherapeutics和Vertex公司聯合開發的CTX001使用CRISPR系統靶向相同的BCL11A基因。去年該公司公布了CTX001在一名嚴重鐮狀細胞貧血患者和一名β地中海貧血患者中的療效。兩名患者的臨床癥狀都有顯著改善。
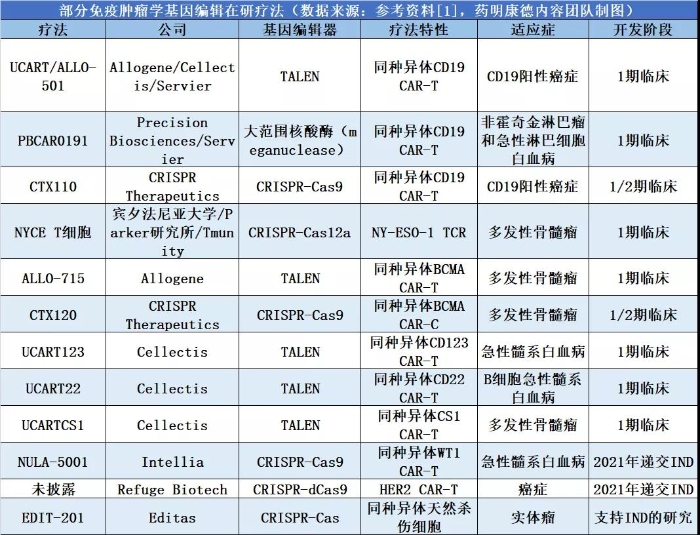
在癌癥免疫療法方面,CAR-T療法的獲批和它們在治療血液癌癥方面的成功,不但為對T細胞進行基因編輯打下了良好的基礎,也為基因編輯技術找出了一個很好的應用領域。CAR-T細胞通過將抗原嵌合受體(CAR)通過基因工程表達在T細胞表面,讓T細胞成為攻擊腫瘤的武器。然而,T細胞中原本存在的天然T細胞受體可能影響CAR-T細胞的療效,并且T細胞還受到多種免疫抑制和調控機制的影響,導致它們功能失常或出現衰竭。
基因編輯技術提供了一種進一步改進CAR-T療法的策略。在2019年,賓夕法尼亞大學的CAR-T療法先驅CarlJune博士與合作伙伴一起,使用CRISPR-Cas9基因編輯技術敲除了T細胞中的內源T細胞受體和表達PD-1的基因。然后,他們將識別NY-ESO-1抗原(一種在多種腫瘤組織中高度表達的抗原)的T細胞受體表達在這些T細胞中。今年2月,研究團隊在《科學》雜志上發表了研究的初步結果。初步結果表明,經過基因編輯的T細胞沒有導致與治療相關的嚴重不良反應,而且顯示出持久的存活和擴增能力。
目前在癌癥免疫療法的研發管線中,基因編輯技術被用于進一步改善靶向CD19或BCMA抗原的CAR-T療法,以及對同種異體細胞療法進行改造,防止同種異體的T細胞對宿主組織進行攻擊。
體內基因編輯研發管線
體內基因編輯療法需要將基因編輯系統送入患者體內,在體內完成對基因組中特定序列的編輯。與體外基因編輯相比,它需要克服更多障礙,而它的應用領域也更為多樣化。
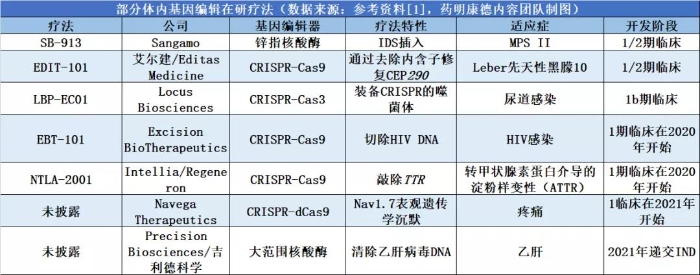
例如,EditasMedicine和艾爾建在今年完成首例CRISPR體內基因編輯療法的患者給藥。這款名為EDIT-101(又名AGN-151587)的在研療法使用腺相關病毒,將CRISPR基因編輯系統導入患者的視網膜細胞中,切除或逆轉導致Leber先天性黑朦10的CEP290基因上的致病突變。
眼睛為檢驗體內基因編輯療法提供了一個良好的環境,因為眼睛屬于免疫特權(immunoprivileged)部位,在眼中引入外來蛋白不容易引起免疫反應,而且眼睛向身體其它部位的血液循環有限,降低基因編輯系統對其它組織進行編輯的風險。同時,被基因編輯的細胞不會更新換代,可能提高基因編輯的長期效果。
今年1月,LocusBiosciences公司宣布,啟動1b期臨床研究,檢驗其武裝了CRISPR-Cas3基因編輯系統的噬菌體crPhage,靶向導致尿道感染的大腸桿菌時的效果。噬菌體是自然界中天然以細菌為食的病毒,然而很多噬菌體殺傷細菌的能力并不算強。LocusBiosciences公司提高噬菌體殺傷力的辦法是給它們裝上CRISPR-Cas3的武器。Cas3與通常的Cas9不同,它一旦識別細菌基因組中的特定序列,會將附近的所有序列切碎,從而達到消滅細菌的效果。在臨床前研究中,這一攜帶CRISPR-Cas3的噬菌體在體外培養和尿道感染的小動物模型中都顯示出更好的殺菌效果。
在基因編輯研發管線中,很多項目治療的疾病為罕見病,這是由于作為一種新興技術,基因編輯的安全性尚未得到完全驗證,因此,在治療沒有已有療法的罕見病患者時的收益/風險比更為合理。不過,隨著更多的臨床試驗結果驗證它的安全性,基因編輯技術有可能向患者人數更多的大眾病擴展。
展望未來
在今明兩年,多項基因編輯臨床項目將公布結果。這些臨床結果將對基因編輯療法的短期未來走向產生很大的影響。同時,研究人員已經在進一步豐富基因編輯的“工具箱”方面取得了重要進步。例如,Broad研究所的劉如謙(DavidLiu)教授基于CRISPR基因編輯系統,開發出單堿基編輯器,能夠將基因序列中的任何堿基修改成其它堿基。這一單堿基編輯系統能夠用于治療多種因為單堿基突變導致的遺傳性疾病。
對基因編輯系統的另一個研發方向是利用它識別基因組序列的能力,不去切斷DNA序列,而是讓它攜帶能夠調控基因表達的調節因子。例如,CRISPR-dCas9系統沒有切割DNA序列的活性,但是它可以與調節基因表達的效應子融合,調節特定基因的表達。NavegaTherapeutics公司希望利用這一工具沉默Nav1.7離子通道的表達,從而阻斷傳遞痛覺信號的通路。
Sangamo公司在去年年底召開的研發日活動中,也著重強調了鋅指蛋白與轉錄因子的結合(ZFN-TF),可以產生精準調節基因表達的工具。該公司還指出,將鋅指蛋白與不同效應子相結合,可以產生行使多種不同功能的基因組調控工具。
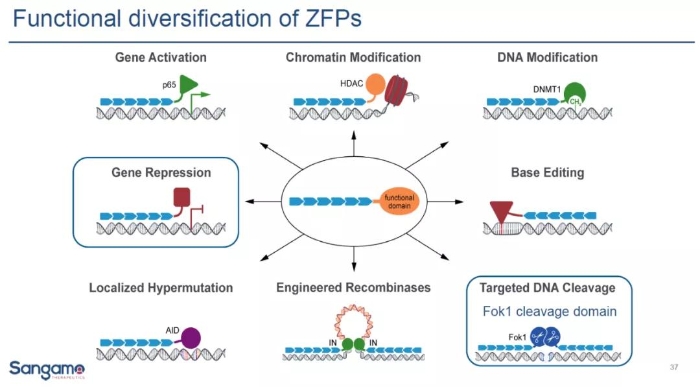
▲鋅指蛋白與不同效應子結合可以產生多種功能
基因編輯技術問世以來,人們對它能夠為治療疾病帶來哪些革新做出了很多設想。在經過多年的努力之后,展現基因編輯療法潛力的臨床試驗結果即將在不久的未來公布,讓我們拭目以待。(藥明康德供稿)
參考資料:
[1]Gene-editingpipelinetakesoff.RetrievedMay19,2020,fromhttps://www.nature.com/articles/d41573-020-00096-y
[2]SangamoR&DDayPresentation.RetrievedMay19,2020,fromhttps://investor.sangamo.com/static-files/e29a38f9-b55b-49c0-b9e5-5240c2165cfd
[3]LocusBiosciencesinitiatesworld’sfirstcontrolledclinicaltrialforaCRISPRenhancedbacteriophagetherapy.RetrievedMay19,2020,fromhttps://www.locus-bio.com/media/locus-biosciences-initiates-worlds-first-controlled-clinical-trial/
本文僅代表作者觀點,不代表本站立場。
《中國醫藥報》社版權所有,未經許可不得轉載使用。
(責任編輯:李碩)
右鍵點擊另存二維碼!
-
為你推薦













