每周醫藥看點(3月2日—8日)
- 2026-03-13 09:31
- 作者:
- 來源:中國醫藥報
國家藥監局綜合司發布通知,部署學習宣傳貫徹新修訂《中華人民共和國藥品管理法實施條例》(以下簡稱《條例》)相關工作;《慢性鼻竇炎伴鼻息肉治療藥物臨床試驗技術指導原則》《抗腫瘤藥物生物等效性及藥代動力學比對研究受試者人群選擇考慮》發布……3月2日—8日,醫藥行業的這些動態值得關注。
行業政策及藥監動態
1.國家藥監局綜合司發布通知,部署學習宣傳貫徹新修訂《條例》。通知要求,各單位要充分認識學習宣傳貫徹《條例》的重要意義;深入學習領會《條例》的立法精神和重點內容;加快制修訂配套文件,確保有效貫徹實施;創新方式方法,積極開展宣傳培訓;夯實監管基礎,加強監管體系和監管能力建設。
2.國家藥監局藥品審評中心(CDE)發布《慢性鼻竇炎伴鼻息肉治療藥物臨床試驗技術指導原則》,旨在指導慢性鼻竇炎伴鼻息肉治療藥物的科學研發和評價,提供可供參考的技術標準。指導原則主要針對慢性鼻竇炎伴鼻息肉治療創新藥物的臨床開發及確證性臨床試驗中試驗設計的關鍵問題,如藥代動力學要求、受試者的入排標準、對照的選擇、用藥周期、療效終點、安全性評價等進行探討,不涵蓋治療慢性鼻竇炎伴鼻息肉的糖皮質激素創新藥物的開發。
3.CDE發布《抗腫瘤藥物生物等效性及藥代動力學比對研究受試者人群選擇考慮》。指導原則主要基于小分子化學藥物及單抗類藥物的研究經驗,為抗腫瘤藥物生物等效性與藥代動力學比對研究中受試者人群的選擇考慮提供建議。
4.CDE就《預防用mRNA疫苗臨床試驗技術指導原則(征求意見稿)》公開征求意見。征求意見稿介紹了mRNA疫苗定義及其特點,先提出針對目標疾病、目標人群、安全性監測和平臺技術等的總體考慮,再對臨床試驗的設計和評價分別進行闡述,最后對上市后研究和平臺技術明確相關重點。
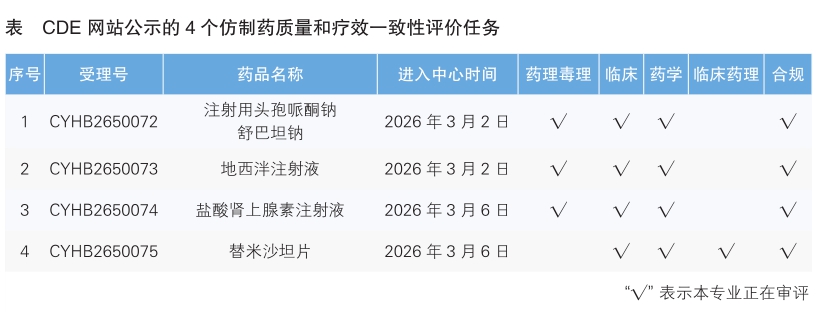
5.CDE網站公示4個仿制藥質量和療效一致性評價任務(詳見表),涉及注射用頭孢哌酮鈉舒巴坦鈉等品種。
產品研發上市信息
1.國家藥監局發布5期藥品批準證明文件送達信息,共包括284個受理號,涉及遠大蜀陽生命科學(成都)有限公司等企業。
2.CDE承辦受理67個新藥上市申請,包括凍干口服輪狀減毒活疫苗(Vero細胞)等。
3.宣泰醫藥宣布,公司維生素K1片的新藥簡略申請已獲得美國食品藥品管理局(FDA)正式批準。
4.藥物牧場宣布,公司針對ROSAH綜合征的試驗性療法DF-003已被納入美國FDA罕見病證據原則(RDEP)認證。
5.瑞初醫藥宣布,公司研發的靶向衰老機制治療眼部疾病的創新藥物RC017,已獲得美國FDA新藥臨床試驗批準。
6.石藥集團宣布,集團開發的SYH2059吸入粉霧劑的新藥臨床試驗申請已獲得美國FDA批準。該藥此次獲批開展臨床試驗適應證為肺纖維化,包括特發性肺纖維化及進展性肺纖維化。
7.同仁堂宣布,公司分支機構同仁堂制藥廠產品右歸丸獲得加拿大產品注冊許可。
醫藥企業觀察
1.德琪醫藥宣布,與優時比達成全球獨家授權協議。根據協議,德琪醫藥授予優時比在全球范圍內推進CD19/CD3雙特異性T細胞連接抗體ATG-201的開發、生產及商業化獨家權益,包括與ATG-201相關的生產技術授權;德琪醫藥將獲得總計8000萬美元的首付款及近期里程碑付款,并有望獲得最高超過11億美元的里程碑付款及基于未來凈銷售額的分級特許權使用費。
2.英矽智能宣布,與阿聯酋藥品管理局簽署戰略合作協議。雙方將通過人工智能賦能的藥物發現與開發等前沿技術,攜手促進阿聯酋醫藥產業發展。
3.星辰集因宣布,與愷佧生物達成戰略合作。根據合作協議,星辰集因授予愷佧生物相關產品的全球生產與銷售權益。雙方將融合星辰集因在底層基因編輯技術上的源頭創新能力,與愷佧生物在原料酶規模化生產、質量體系及全球商業化推廣的產業經驗,共同推動新型基因編輯技術的產業化進程與商業化應用。
4.科絡思生物宣布,與同宜醫藥簽署戰略合作協議。根據協議,雙方將在三大方向展開系統性合作:一是聚焦具有差異化競爭力的創新管線開展聯合開發與成果共享;二是整合雙方研發與商務拓展資源,共同推進重點項目的全球商業化拓展;三是在資本層面探索多元合作機制,推動產業與資本協同發展,提升整體戰略效率與價值創造能力。
5.中國生物制藥宣布,與賽諾菲就JAK/ ROCK抑制劑羅伐昔替尼達成獨家授權協議。根據協議,中國生物制藥子公司正大天晴授予賽諾菲在全球范圍內開發、生產及商業化羅伐昔替尼的獨家許可。中國生物制藥有權獲得最高15.3億美元的付款,其中包括1.35億美元的首付款,以及后續潛在開發、監管和銷售里程碑付款;同時,中國生物制藥還可按羅伐昔替尼年度凈銷售額,收取最高雙位數比例的階梯式特許權使用費。
藥品集中采購
1.河北省醫用藥品器械集中采購中心發布通知稱,擬開展聯盟(省)集采到期部分藥品接續集中采購,包括蛋白琥珀酸鐵等8個品種。河北省各級公立醫療機構、軍隊醫療機構和門診保障定點藥店是本次集采藥品的采購主體;本次集采中選藥品自執行之日起,兩年為一個采購周期,采購周期內采購協議每年一簽。
2.江西省醫保局、省衛生健康委、省藥監局三部門聯合發布《關于進一步規范緊密型縣域醫共體藥品和醫用耗材統一采購工作的通知》。通知明確,醫共體須達到緊密型醫共體建設評判標準,并已實施醫保基金總額“打包”付費管理;醫共體總醫院或牽頭醫院為藥品和醫用耗材統一采購的責任主體,統籌管理醫共體內所有成員單位的藥品和醫用耗材采購、配送、結算、追溯及調劑等工作。此外,醫共體按照“十統一”原則(統一賬號、統一目錄、統一需求、統一采購、統一配送、統一結算、統一追溯、統一調劑、統一考核、統一信息),規范藥品和醫用耗材采購流程。
3.上海市醫藥集中招標采購事務管理所發布《關于進一步完善本市掛網藥品價格風險預警標識的通知》。通知明確,將對生物藥(生物制品+生物類似藥)合并歸類,風險標識調整為:以同種藥品最低掛網價的3倍為黃標價格,最低掛網價的5倍為紅標價格。此外,自今年第四季度起,對醫療機構采購行為按季度實施監測,相關結果納入醫療機構考核范圍,重點關注采購“紅標”藥品金額占比超過10%,或采購“紅黃標”藥品累計金額占比超過25%的醫療機構。(劉鶴整理)
《中國醫藥報》社版權所有,未經許可不得轉載使用。
(責任編輯:劉思慧)
右鍵點擊另存二維碼!
-
相關閱讀
-
為你推薦