加快標準制定 助力新技術在醫療器械領域高質量運用 ——醫用增材制造醫療器械全生命周期質量控制和行業標準建設進展
- 2021-10-21 15:49
- 作者:韓倩倩 王春仁 李靜莉
- 來源:?中國食品藥品網
當新技術應用到醫療器械研發生產中時,要關注因新技術引發的新風險,應用標準的方法來評估風險、評價產品的安全有效性,盡可能在現有技術條件下消除風險,保障新技術的安全應用至關重要。因此,要科學制定基于新技術研發生產的醫療器械的質量評價標準,使新技術在發展之初便得到標準化工作的支撐。有了標準的支撐,一方面可以使新技術更好更快地用于產品制造;另一方面可以縮短產品的研發、驗證、臨床應用的總體轉化時間。在醫療器械新技術應用領域,我國有望實現國際醫療器械研發制造的彎道超車,所以加強基于新技術研發生產的醫療器械的標準化研究有助于產品上市前的科學把關、落實前瞻性全生命周期監管、規范產業發展。
增材制造技術應用于醫療器械的研發制造是新技術應用的范例。因增材制造技術涉及數據建模、醫工交互、個性化定制等環節,所以產品的全生命周期質量管理尤為重要。2021年3月,國家藥品監督管理局、國家標準化管理委員會發布了《關于進一步促進醫療器械標準化工作高質量發展的意見》,鼓勵開展增材制造醫療器械領域的標準化工作。
國家藥監局2019年批準組織成立醫用增材制造技術醫療器械標準技術歸口單位,中國食品藥品檢定研究院作為歸口單位秘書處承擔單位,通過開展技術研究和組織標準制定,現階段已經制定發布國家藥監局行業標準兩項,預研行業標準提案13項,建立了覆蓋全生命周期質量控制環節的醫用增材制造技術醫療器械行業標準體系。
行業標準研究先行 奠定產品高質量發展標準化基礎
增材制造技術將生物醫用材料、工程、數據、醫學個性化需求交叉匯融,近年得以逐步廣泛應用。增材制造醫療器械產品類型包括醫療用模型、手術導板、骨科產品、組織修復產品、血管植入物、矯形器具等。國家藥監局數據顯示,截至目前,共有14個增材制造技術產品獲得注冊證。主要代表性產品有作為三類醫療器械管理的增材制造髖關節假體、頸椎融合器、骨盆缺損匹配假體;作為二類醫療器械管理的增材制造骨模型、截骨導板、種植牙定位導板等。已經進入臨床研究的代表產品有增材制造純坦骨科植入物、增材制造鎳鈦合金骨科植入物和增材制造陶瓷骨科植入物等。增材制造應用于醫療器械的制造具備獨特的個性化實現和精密微觀結構實現的優勢,同時也引來了獨有的風險。比如粉末狀原材料質控缺乏技術指標,設備驗證關鍵生產環節缺乏規范要求,成品檢測方法匱乏等。所以,該領域的發展急需風險分析技術、質量控制技術和標準化工作的指導。
面對技術變革,中國食品藥品檢定研究院開展了醫用增材制造醫療器械的檢驗技術和標準化技術研究,建立了涵蓋原材料、工藝驗證、設備、數據傳輸和風險管理的標準體系,并開展行業標準的制定。
從支撐全生命周期監管的角度,中國食品藥品檢定研究院對涉及產品安全有效的各個環節展開研究,確定了十大關鍵技術和標準化環節,分別是產品設計、原材料質量控制、醫工交互、數據建模、設備參數控制、打印后處理、成品質量控制、臨床實用、上市后隨訪、取出物分析。針對各個環節征集標準立項提案,共預研了13項行業標準提案,其中目前已經制定發布了增材制造技術的基礎性原材料標準YY/T1701-2020《用于增材制造的醫用Ti-6Al-4V/Ti-6Al-4VELI粉末》、YY/T1809-2021《醫用增材制造粉末床熔融成形工藝金屬粉末清洗及清洗效果驗證方法》,2021年度組織制定行業標準YY/TXXXX《用于增材制造的醫用純坦粉末》。
著眼全生命周期質量控制 構建覆蓋全環節的行業標準體系
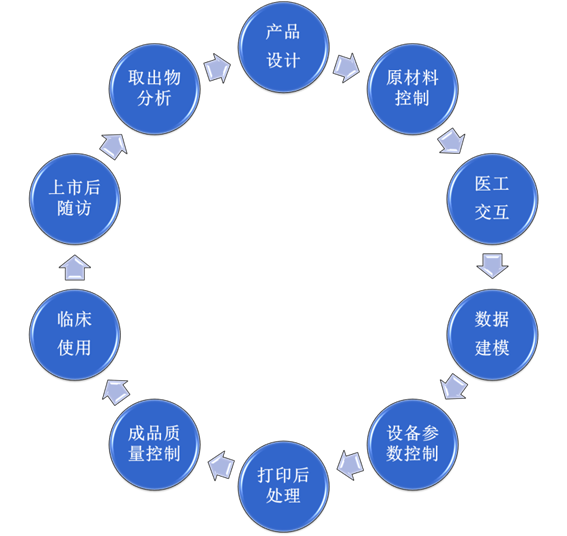
完善的標準是質量可控的重要保障之一。根據增材制造醫療器械的特點,歸口單位秘書處研究建立了10個質量控制及標準技術研究環節(如圖所示)。只有各個環節都做到滿分,才能達到成品的質量可控。
圖.增材制造醫療器械全生命周期質量控制和標準化關鍵環節
(1)產品設計:增材制造醫療器械的設計包含外形設計和內部結構設計。增材制造醫療器械的臨床應用優勢是可以進行個性化定制,即根據患者的特殊病損進行設計。以骨植入類產品為例,可以設計獨特的三維精密結構以增加其骨整合性,好的設計使骨整合更好地發揮功能,更符合患者的個體特點。針對產品設計,現階段已經有預研標準2項:骨植入物設計流程和骨科外固定器械仿生結構合理性評價。
(2)原材料控制:原材料的質量控制是打印產品質量的基礎。金屬增材制造原材料是球形粉末狀,如金屬粉末、光敏樹脂粉末、高分子粉末、陶瓷粉末等,對金屬粉末原材料進行質量控制是保證增材制造產品質量的基礎。增材制造原材料應建立符合醫療器械生產需求的表征指標。針對醫用增材制造技術醫療器械的特殊要求,歸口單位著力制定不同種類醫用增材制造技術原材料的專用要求。目前已發布1項鈦合金粉末標準——YY/T1701-2020,1項坦粉末標準2021年底報批;預研形成2項生物陶瓷原材料標準提案:β-磷酸三鈣粉末、羥基磷灰石粉末。
(3)醫工交互:醫工交互是實現增材制造醫療器械的關鍵。醫工交互是指醫生與生產企業的工程技術人員的有效溝通,并根據數據進行合理建模和設計。醫生需針對患者的臨床需求和適用性做出判斷,準確采集臨床數據。這些數據是建模的基礎。
(4)數據建模:醫用增材制造技術數據建模控制環節的數據建模環節包括數據傳輸的安全性和有效性、數據處理方法的準確性、建模方法穩定性和準確性。目前,歸口單位已經預研了醫工交互平臺建設的基本要求標準。
(5)設備參數控制:打印設備是實現增材制造醫療器械生產的重要硬件。設備運行的穩定性和打印工藝的穩定性決定了產品的批間差異是否在可接受范圍內。打印設備的打印參數要有嚴格的驗證程序,確保打印工藝的可實現性和穩定性。有必要針對不同成型工藝的要求,如擠出式、能量直接沉積、激光熔融等建立專用于增材制造醫療器械的打印設備的通用要求和專用要求、設備參數運行穩定性的驗證方法、設備改裝控制方法等。歸口單位已經征集到2項預立項研究提案:粉末床電子束熔融工藝控制與確認、PEEK熔融沉積增材制造穩定性。
(6)打印后處理:打印的初步產品需經過必要的后處理,如消除熱應力、表面粗糙度處理、去除粉末殘留等。這些后處理是產品的合理力學性能和生物相容性的重要保證。針對加工工藝穩定性驗證,已經制定發布了YY/T1809-2021醫用增材制造粉末床熔融成形工藝金屬粉末清洗及清洗效果驗證方法。
(7)成品質量控制:成品質量控制方面需要根據增材制造所帶來的特殊風險展開研究,建立針對醫用增材制造技術的專用測試方法,包括機械測試方法,如力學測試方法和非破壞性測試方法;化學特性測試方法,如晶型結構成分檢測方法;生物學特殊風險評價方法,如仿生結構合理性評價方法和微粒的毒理學效應評價方法。
(8)臨床應用:對于罕見特殊病損所需的定制式增材制造醫療器械,在按照《定制式醫療器械監督管理規定(試行)》實行備案制管理的基礎上,還應加強各個環節所需具體實施規范的研究。醫療機構應當建立定制式醫療器械查驗記錄制度,定制式醫療器械的制作訂單,產品驗收、調改、使用、退回等信息以及與使用質量安全密切相關的必要信息妥善保存,確保信息具有可追溯性,并在病歷中記錄定制式醫療器械產品名稱和唯一識別編號。醫療機構應當對使用后的定制式醫療器械開展評價工作。由醫療、護理、臨床工程技術、醫院感染控制、生產企業技術人員等組成評價工作技術團隊,對定制式醫療器械使用的實際效果和質量安全情況進行分析評價,并將此評價結果作為后期合理使用的重要依據。
(9)上市后隨訪:針對植入人體后的增材制造醫療器械,要加強隨訪。醫療機構應當制定完善的安全防范措施和風險控制計劃,發生嚴重不良事件等緊急情況時,立即啟動應急預案,采取防范控制措施,及時處置。
(10)取出物分析:如遇不良事件需取出植入物時,要建立取出的操作流程和取出后產品的測試分析技術,找出產品失效原因。
全行業加強聯動 構筑新技術安全有效應用的有利環境
產、學、研、檢、醫、標準化研究機構和監管部門各個環節的密切配合,是增材制造醫療器械安全有效應用的保障。在全行業聯動的過程中,標準也是鏈接各個環節的重要技術“語言”。
因增材制造技術應用于醫療器械生產仍缺乏經驗,研發機構要加強打印技術原理的研究,開發更適合的原材料和精密度更高且擁有自主知識產權的設備和建模軟件。生產者要做好生產管理,提高打印精密度和可控性。面對增材制造技術人才和醫工交互人才匱乏的現狀,有必要在高校或職業學校設立相關專業,培養產業工人和技術人才。檢測研究機構承擔增材制造醫療器械的質量評價,需要加大檢測方法和工藝驗證方法的研究。標準化研究機構要加強該領域的標準化研究,研制急需的標準,使產品研發和驗證有據可依。法規制定部門也應緊密追蹤技術和產業發展趨勢,制定適合的監管法規,規范產業發展。
只有加強全行業聯動,共同貢獻智慧和經驗,才能使新技術在醫療器械領域的應用達到安全、有效、質量可控。(作者單位:中國食品藥品檢定研究院)
《中國醫藥報》社版權所有,未經許可不得轉載使用。
(責任編輯:辛悅然)
右鍵點擊另存二維碼!
-
為你推薦
互聯網新聞信息服務許可證10120170033
網絡出版服務許可證(京)字082號
?京公網安備 11010802023089號 京ICP備17013160號-1
《中國醫藥報》社有限公司 中國食品藥品網版權所有