2022年12月份抗代謝藥物和激素拮抗劑新開臨床試驗數量增長明顯
- 2023-02-20 10:38
- 作者:陳宇哲
- 來源:中國醫藥報
根據美國Clinicaltrial數據庫數據,2022年12月份全球新增由企業資本主導的臨床試驗總數為774項,新開臨床試驗數量顯著上升,較上月增長8.56%,較2021年同期增長0.39%。
2022年12月份,新開臨床試驗數量最多的企業(機構)是諾華制藥,申報數量為20項,相較于上月增幅為185.71%;其次為輝瑞,新開臨床試驗數量為19項。值得注意的是,捷邁邦美(Zimmer Biomet)公司首次進入全球單月新開臨床試驗數量前十名公司序列,本月新開展臨床試驗11項。捷邁(Zimmer)公司由J.O.Zimmer于1927年創立,2015年完成對邦美(Biomet)公司的收購,該公司一直致力于骨科醫療保健領域產品的研發。
對比前三名臨床試驗申報大企業(諾華、輝瑞、阿斯利康)在臨床適應癥和藥物類型方面的分布可知,研究最熱也是競爭最為激烈的領域是免疫系統疾病領域。在該領域,輝瑞共開展3項臨床試驗,其中一項為口服JAK1抑制劑阿布昔替尼片(Abrocitinib)的觀察性研究(NCT05391061),一項為針對于彌漫性大B細胞淋巴瘤適應癥的PF-07901801(CD47靶蛋白)的Ⅱ期臨床試驗(NCT05626322),以及一項針對多發性骨髓瘤適應癥的雙抗新藥Elranatamab的Ⅰ期臨床試驗。
該月,諾華在免疫系統疾病領域的新增臨床試驗數量最多,有7項,且有4項已經處于Ⅲ期臨床試驗階段,其中一項已進入患者招募狀態。處于患者招募狀態的Ⅲ期臨床試驗(NCT05648968)的主要適應癥為溫抗體型自身免疫性溶血性貧血(wAIHA),試驗藥物為生物藥Ianalumab(VAY736),是一種耗竭B細胞、阻斷B細胞活化因子受體的單克隆抗體。在其他3項Ⅲ期臨床試驗中,有兩項的試驗藥物仍為Ianalumab,適應癥均為原發性免疫性血小板減少癥(TTP),其中一項試驗(NCT05653219)的陽性對照藥為曲波帕/艾曲博帕(Eltrombopag),另一項試驗(NCT05653349)的陽性對照藥為皮質類固醇Corticosteroids;還有一項Ⅲ期臨床試驗(NCT05513001)為Remibrutinib在慢性自發性蕁麻疹患者中長期療效、安全性和耐受性的擴展研究。其余3項臨床研究均為觀察性研究。
阿斯利康在免疫系統疾病領域的新增臨床試驗數量為3項,均為觀察性研究,適應癥分別為:哮喘(NCT05677139)、既往未治療的慢性淋巴細胞白血病(NCT05665374),以及慢性淋巴細胞白血病(NCT05645172)。
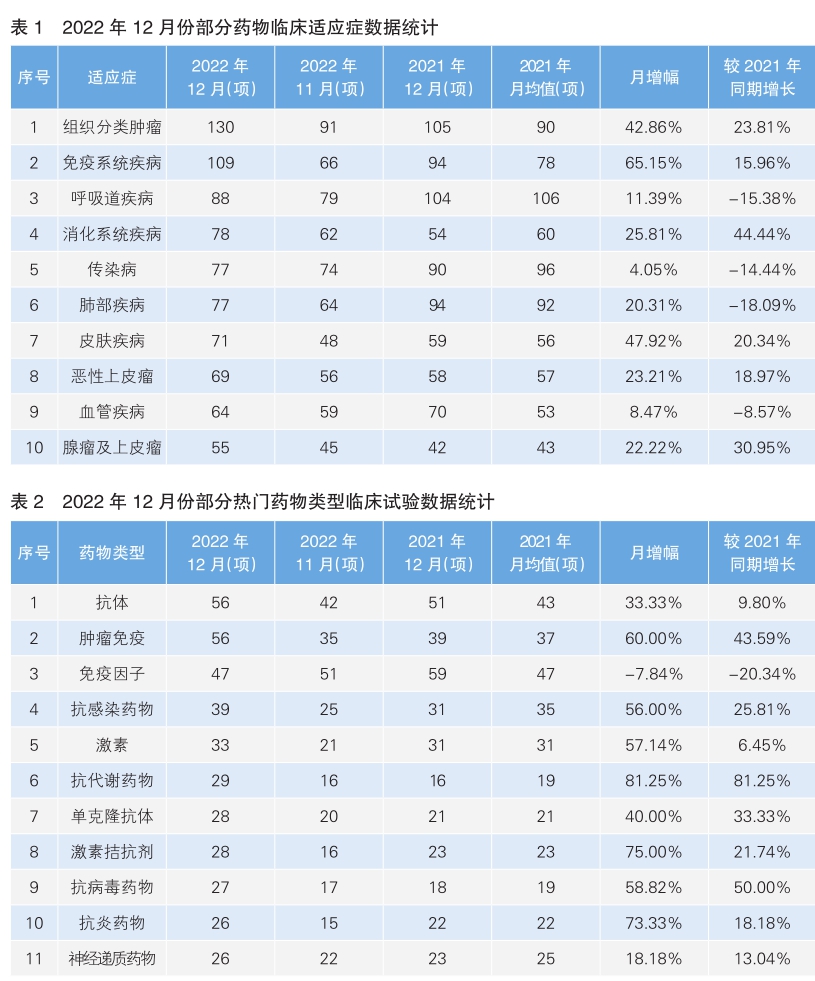
從全球新開臨床試驗適應癥來看,組織分類腫瘤仍為其中最熱門的研發領域,試驗數量為130項,較上月增加42.86%;其次為免疫系統疾病,較上月增加65.15%,是月增幅最高的熱門適應癥領域。試驗數量下降最為顯著的領域為呼吸道疾病和肺部疾病,兩者降幅均超過15%。(詳見表1)
全球熱門藥物類型臨床試驗數量大多呈現上升趨勢,增幅較大的藥物門類為抗代謝藥物和激素拮抗劑,較上月分別增長81.25%和75.00%;熱門藥物類型中僅有免疫因子的臨床試驗數量出現下降,較上月下降7.84%,相較于去年同期水平下降20.34%。(詳見表2)
對臨床試驗的申請國家及地區進行統計后發現,美國仍為當月新開臨床試驗最多的國家,其次是中國。相較于上月,除美國和加拿大以外,其他臨床試驗申報的熱門地區新開展臨床試驗數量均呈下降趨勢,降幅較明顯的為德國和澳大利亞,分別下降30.61%和46.67%。
(數據來源于美國Clinicaltrial數據庫,標簽間存在統計重復,統計時間為2023年1月10日)
《中國醫藥報》社版權所有,未經許可不得轉載使用。
(責任編輯:陸悅)
右鍵點擊另存二維碼!
-
為你推薦