進口仿制雙輪驅動?多維協同回應急需 ——盤點2022年我國罕見病藥物加速獲批上市情況
- 2023-02-27 10:59
- 作者:孫潭霖
- 來源:中國醫藥報
黨的二十大報告指出,必須堅持在發展中保障和改善民生,推進健康中國建設,把保障人民健康放在優先發展的戰略位置。在我國,罕見病總體人群數量龐大、疾病負擔重,該領域正越來越引起政府和社會的廣泛關注。為維護患者健康權益,加強罕見病管理,提高診療水平,我國政府出臺多項政策措施,鼓勵罕見疾病藥物的引進、研發、申報和生產。2018年發布的《第一批罕見病目錄》(以下簡稱《目錄》)為優化罕見病藥物研發環境奠定了基礎。然而,我國罕見病藥物研發起步較晚,政策長期空白,市場存在不確定性,企業研發動力不足,罕見病藥物獲批數量較少。
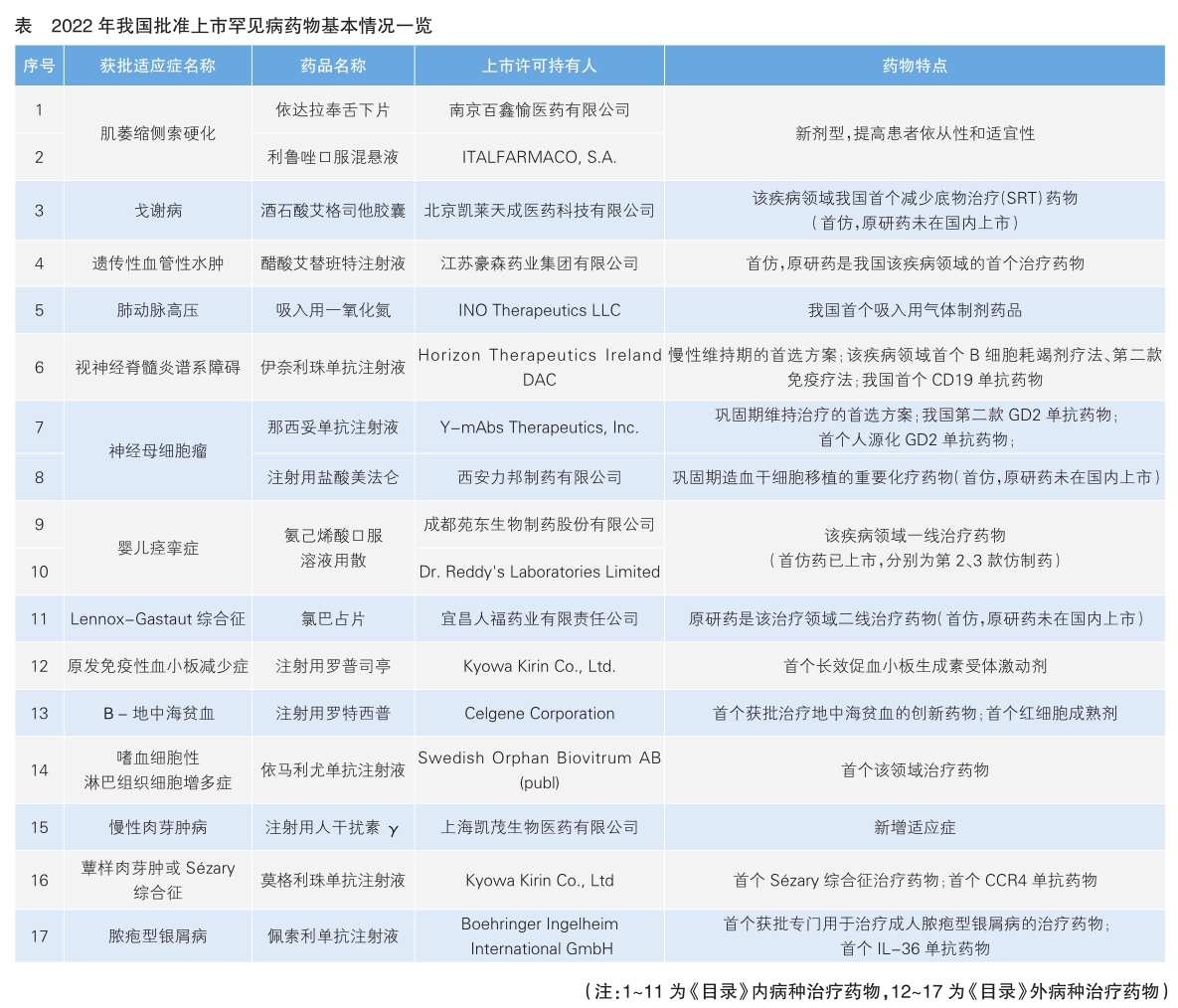
2022年蔻德罕見病中心和艾昆緯聯合發布的《共同富裕下的中國罕見病藥物支付》報告顯示,全球共有7000多種罕見病,然而“有藥可治”的罕見病病種僅有85個,中國“境內有藥”的罕見病病種僅有68個。自2020年起,我國每年獲批上市罕見病藥物數量均超過15個,2022年共有17個罕見病藥物獲批上市。
本文試對國家藥監局2022年批準的罕見病藥物進行回顧和盤點。
產業發力
豐富罕見病藥物類型
與往年相比,2022年我國批準上市的罕見病藥物具有仿制藥占比高、明確兒童適應癥的藥品占比高、國內企業參與形式多樣、覆蓋疾病種類多樣等顯著特點。
進口仿制雙輪驅動,滿足多方面臨床需求
一是批準藥品種類多,全年共批準進口藥10個、國產仿制藥6個、改良型新藥1個。其中,生物制品8個、化學藥品9個。二是覆蓋多個重點領域,涉及神經、代謝、血液、心血管、皮膚等多種疾病治療領域,明確包含兒童適應癥的藥品有11個。其中,《目錄》內病種治療藥物11個。《目錄》外病種治療藥物6個。三是多方面滿足需求,4個進口藥品直接填補我國相關疾病治療領域臨床空白,如依馬利尤單抗是嗜血細胞性淋巴組織細胞增多癥的首個治療藥物;2個進口藥品提供了疾病關鍵期內的治療方案,如伊奈利珠單抗主要用于治療視神經脊髓炎譜系障礙,是慢性維持期的首選方案;3個新劑型提高了用藥依從性和適宜性,如依達拉奉舌下片可以降低醫療資源占用,減少并發癥,臨床應用風險更可控,且用藥方便,可以拓展更多治療方案;3個首仿藥品提高了藥品可及性,如醋酸艾替班特的原研藥是遺傳性血管性水腫治療領域的首個藥物,費用高昂,仿制藥獲批后,原研藥價格降低了48%。
國內企業積極參與罕見病藥物研發、上市和商業化推廣
長期以來,我國上市的大多數罕見病藥物以進口為主,國產藥研發主要集中在血友病凝血因子、凝血酶原相關藥物。但從2022年獲批的藥品來看,國內企業積極承擔社會責任,基于自身情況尋求差異化發展和布局,從不同賽道切入關注這一既往極少關注的人群。國內涌現了如李氏大藥廠等企業,與境外中小型企業合作,引進開發和商業化多種境外已上市罕見病藥品,同時這些企業也積極研發改良型新藥、仿制藥,多維度滿足患者需求。
政策賦能
釋放藥審改革紅利
2022年罕見病藥物的加速獲批是深化藥審改革的成果。同時,多部門聯合發力,制定發布了鼓勵仿制藥品目錄、鼓勵研發申報兒童藥品清單、臨床急需境外新藥審評審批工作程序,為罕見病藥物的審評審批、進口通關、醫保準入、進院使用、知識產權保護等提供了有力保障,協同助力藥品滿足臨床需求。
接收境外臨床試驗數據,加速臨床急需藥物批準
境外已上市藥品的進口或仿制,是解決我國患者臨床迫切需求藥品可及性的重要手段。2020年起,國家藥監局藥品審評中心(CDE)發布了多項境外已上市境內未上市藥品藥學、臨床試驗等相關指導原則,有利于避免重復開展臨床試驗,降低研發成本,促進境內外企業合作。2022年獲批的進口罕見病藥品絕大多數豁免境內臨床試驗,境內外上市時間差約為3年。跨國藥企也選擇在我國同步布局多中心臨床試驗,進一步加速藥品同步上市。如佩索利單抗是首個獲批的進口1類生物藥,企業在國際多中心臨床試驗結束后同步向中國、美國和歐洲提交上市申請,我國批準時間僅比全球首次批準(美國)晚100天。
制定指導原則,兼顧兒童用藥開發
絕大多數罕見病為遺傳疾病,且多在兒童生長發育關鍵期發病,病情隨年齡進展,成為患者和家庭長期沉重的疾病負擔。兒童患者生理復雜性和臨床試驗招募難等困境加劇了這一領域罕見病藥物的研發。近年來CDE完善審評標準體系、加強溝通與交流,發布多項罕見病用藥、兒童用藥等技術指導原則。2022年獲批的多數罕見病藥物的適應癥明確包含兒童人群。
急用先行,優先分配技術和審評資源
藥品監管部門針對不同類別的藥物建立了多條快速通道或成立工作組,推進臨床急需藥物進一步加速上市惠及患者。“快速通道”和臨床急需境外新藥審評審批工作程序為罕見病藥物、兒童用藥、臨床急需藥物等開辟“綠色通道”,合理配置審評資源,實現藥品“急用先行”。仍以佩索利單抗為例,其在中歐同步提交上市申請,但在我國獲批先于歐洲。
展望未來
罕見病藥物研發機遇與挑戰并存
首先,從全球來看罕見病藥物仍有大量未被滿足的需求。例如嬰兒痙攣癥和肌萎縮側索硬化癥,2022年獲批的4款藥品均為對癥治療,全球也尚無從源頭根治的藥物。嬰兒痙攣相關疾病雖然有一些明確的致病基因,但境內還沒有基因療法的相關研究,境外也僅有少數藥品進入到臨床試驗階段;90%的肌萎縮側索硬化患者發病原因尚不明確,亟需從基礎研究層面突破。從產業角度來看,建議企業既要探索支持自身持續發展的經營之路,也要完成自主創新升級,真正以臨床價值為導向,加強基礎研究和合作,填補更多臨床空白,或為患者提供更多選擇。
其次,逐步突破《目錄》限制,建立適宜的罕見病定義。2022年獲批的《目錄》外病種治療藥品相對《目錄》內病種治療藥品的數量少、納入醫保的比例較小,缺少“清單”類政策支持。全球罕見病達7000多種,《目錄》囊括病種有限,意味著《目錄》外罕見病的患者和治療藥物無法享有相關激勵政策和待遇,不利于實現公平性和保障患者健康權。罕見病目錄不應成為“定義罕見病”的目錄,應探索以患病率或患病人數等角度定義罕見病,使滿足條件的藥品即獲得相應資格并適用相應政策。
最后,還需要多部門協同進一步激勵獲得罕見病資格的藥品研發并惠及患者。近年來,我國已由多部門聯合出臺相關政策在進口罕見病藥品方面發力,但仍需進一步建立適應中國國情的罕見病及藥物研發激勵機制,在國家層面制定相關政策進一步對獲得罕見病資格的藥品在研發、審評、醫保準入方面予以支持。如在藥品監管層面,落實藥品試驗數據保護和罕見病用藥市場獨占期制度;在醫保層面,盡快探索建立罕見病藥物的準入、價值評估方法、支付方式和多層次保障體系。
令人振奮的是,我國很多新興生物技術企業已經開始布局罕見病領域,在中國開展的部分罕見病作用機制藥物臨床試驗已經實現國際同步或全球領先。期待在政府、企業、患者和社會的多方努力下,我國更多原創罕見病藥物盡早惠及中國和全球患者。
(中國醫藥創新促進會政策研究中心研究員 孫潭霖)
《中國醫藥報》社版權所有,未經許可不得轉載使用。
(責任編輯:陸悅)
右鍵點擊另存二維碼!
-
為你推薦