每周醫藥看點(1月26日—2月1日)
- 2026-02-03 15:40
- 作者:
- 來源:中國食品藥品網
國家藥監局發布《仿制藥參比制劑目錄(第一百零一批)》,其中包括甲磺酸加諾沙星片等品種;國家藥監局綜合司印發《2026年藥品檢驗能力驗證計劃》,包含水楊酸片溶出度測定能力驗證計劃等項目……1月26日—2月1日,醫藥行業的這些動態值得關注。
行業·政策動態
1.國家藥監局發布《仿制藥參比制劑目錄(第一百零一批)》,其中包括甲磺酸加諾沙星片等品種。
2.國家藥監局綜合司印發《2026年藥品檢驗能力驗證計劃》,旨在提升藥品、醫療器械、化妝品檢驗機構能力和水平。該計劃包含水楊酸片溶出度測定能力驗證計劃等項目,由中國食品藥品檢定研究院負責組織實施。
3.國家醫保局辦公室、國家中醫藥管理局綜合司聯合發布通知,通過遴選,確定將北京、河北等9個省份以及內蒙古通遼、遼寧沈陽等9個城市納入中醫優勢病種按病種付費試點。
4.國家藥監局藥品審評中心(CDE)發布《化學藥品創新藥晶型研究技術指導原則(試行)》,明確創新藥晶型研究過程中的關注點及一般原則。該指導原則適用于化學藥品創新藥的晶型研究,改良型新藥晶型的研究可參考進行。
5.CDE發布《用于術后鎮痛的長效局部麻醉藥臨床試驗技術指導原則(試行)》,規范此類藥物的臨床試驗設計,提高研發的質量與效率。該指導原則重點針對用于術后鎮痛的創新和改良型長效局部麻醉藥的Ⅲ期試驗的關鍵設計要素提出相關考慮(并未包含試驗方案的全部設計要素),同時提出臨床試驗中的其他關注點。。
6.CDE發布《細胞治療藥品藥學變更研究與評價技術指導原則(試行)》,指導申請人/持有人科學地開展細胞治療藥品藥學變更研究,規范細胞治療藥品全生命周期的研究與管理。
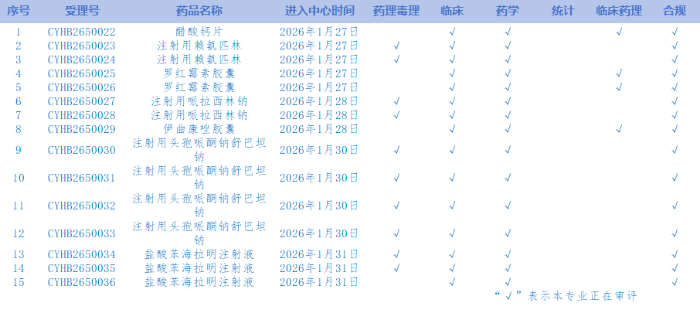
7.CDE網站公示15個仿制藥質量和療效一致性評價任務(詳見表),涉及醋酸鈣片等品種。
產品研發·上市信息
1.國家藥監局發布4期藥品批準證明文件送達信息,共包括329個受理號,涉及華輝安健(北京)生物科技有限公司等企業。
2.CDE承辦受理63個新藥上市申請,包括金柴膠囊等。
3.信達生物宣布,其抗GPRC5D/BCMA/CD3三特異性抗體IBI3003獲得美國食品藥品管理局(FDA)授予的快速通道資格。IBI3003擬定適應證為接受過含一種蛋白酶體抑制劑、一種免疫調節藥物及一種抗CD38單抗的至少四線治療的復發或難治性多發性骨髓瘤。
4.藥物牧場宣布,其ALPK1抑制劑DF-003獲得FDA授予的快速通道資格。DF-003擬用于治療ROSAH綜合征。
醫藥企業觀察
1.先聲藥業宣布,與勃林格殷格翰達成一項協議。雙方將共同開發先聲藥業的TL1A/IL23p19雙特異性抗體SIM0709,用于炎癥性腸病的治療。根據協議,勃林格殷格翰獲得該項目在大中華區以外的全球權益;先聲藥業可獲得首付款,以及基于開發、注冊和商業里程碑付款,最高可達10.58億歐元。
2.石藥集團宣布,與阿斯利康簽訂戰略研發合作與授權協議,利用石藥集團的緩釋給藥技術平臺及多肽藥物AI發現平臺,開發創新長效多肽藥物。根據協議,石藥集團將授予阿斯利康對相關授權產品在全球范圍(不含中國)開發、生產和商業化的獨家權益;石藥集團將獲得12億美元的預付款,并有權獲得最高35億美元的潛在研發里程碑付款和最高138億美元的潛在銷售里程碑付款。
3.藥明生物宣布,與生諾醫藥達成戰略合作協議。根據協議,生諾醫藥將借助藥明生物在生物藥開發和生產領域積累的豐富經驗和規模化生產能力,推進SND006的臨床前藥學研究和臨床樣品制備,加速臨床申報進程。SND006系生諾醫藥自主研發、享有全球權益的雙特異性抗體,擬用于治療炎癥性腸病等自身免疫性疾病。
4.英矽智能宣布,與齊魯制藥集團及其下屬上海齊魯制藥研究中心達成藥物研發戰略合作。根據協議,英矽智能將利用自主搭建的Pharma.AI平臺,關注用于代謝疾病領域的新穎小分子藥物設計與優化;齊魯制藥集團將負責后續開發與商業化工作。
5.東陽光藥宣布,與晶泰科技達成戰略合作。雙方將聚焦自身免疫性疾病領域,結合東陽光藥的全鏈條研發經驗與晶泰科技的AI藥物研發技術,加速候選藥物的發現與臨床轉化;雙方還將以“算力+數據+生態”模式共建AI超算平臺,向學界與產業界開放合作成果,推動數據資產與AI產品向“模型即服務”商業模式轉化。
藥品集中采購
河北省醫用藥品器械集中采購中心發布通知,公布河北省聯盟(省)集采到期接續藥品集中采購中選結果。中選結果包括北京凱因科技股份有限公司的復方甘草酸苷等390款藥品。通知明確,接續藥品中選企業仍為原中選企業的,中選企業需繼續供應并按新的中選價簽訂三方協議,協議自2026年1月1日執行。此次中選結果部分更換或全部更換的,原中選企業應繼續供應,新中選企業要結合實際,積極做好備產備供,中選結果自2026年3月1日起執行。(劉鶴整理)
《中國醫藥報》社版權所有,未經許可不得轉載使用。
(責任編輯:劉思慧)
右鍵點擊另存二維碼!
-
相關閱讀
-
為你推薦