王擁軍院士團隊TASTE-2研究登上《英國醫學雜志》 腦細胞保護劑聯合取栓顯著降低致殘
- 2026-01-09 15:04
- 作者:木子
- 來源:中國食品藥品網
中國食品藥品網訊 近日,中國卒中治療研究取得重大進展。由首都醫科大學附屬北京天壇醫院王擁軍院士團隊牽頭完成的一項針對缺血性卒中患者的大規模臨床研究(TASTE-2),在國際頂級醫學期刊《英國醫學雜志》(BMJ,IF:42.7)上正式發表全文結果。研究證實,在標準的血管內取栓治療(EVT)基礎上,聯用國產創新藥依達拉奉右莰醇,可顯著提升急性大血管閉塞性卒中患者90天的功能獨立比例,且安全性良好。這標志著由中國學者領銜的“腦細胞保護+再灌注”聯合治療方案,獲得了國際學術界的高級別認可,為全球卒中治療提供了新的“中國方案”。

TASTE-2研究2026年1月7日發表于BMJ雜志
卒中是我國成年人致死、致殘的首位病因,其中約70%為缺血性卒中(AIS)。目前,急性缺血性卒中治療已進入“再灌注時代”,血管內取栓是救治大血管閉塞患者的“金標準”。盡管取栓術能實現高達70%-90%的血管再通,但仍有近一半的患者留下不同程度的殘疾。如何進一步保護缺血腦組織、降低卒中致殘,仍是全球面臨的臨床難題。
國際權威學術組織STAIR曾提出,缺血性卒中治療中理想的腦細胞保護策略應能多靶點干預缺血損傷,并與再灌注治療聯合。由中國自主研發的多靶點腦細胞保護劑依達拉奉右莰醇率先在該領域獲得成功的臨床驗證。
該大規模隨機雙盲對照試驗在中國106家中心開展,共納入1362名患者。所有患者均在發病24小時內接受取栓治療,并隨機分組,在取栓前開始接受依達拉奉右莰醇或安慰劑治療,持續約兩周。
研究主要目標是評估患者90天后的功能獨立(改良Rankin量表評分0-2分,即恢復完全生活自理能力)的情況。最終數據顯示,相較于安慰劑組,依達拉奉右莰醇顯著改善了患者90天功能獨立結局,且兩組在嚴重不良事件、死亡率等安全性指標上無顯著差別。
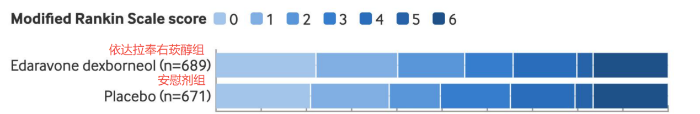
TASTE-2結果顯示,患者治療后恢復功能獨立(90天mRS 0~2分)比例上,依達拉奉右莰醇組(55.0%)與安慰劑組(49.6%)相比有顯著提高(P=0.047)
值得注意的是,亞組分析顯示,入院時影像學與臨床癥狀不匹配的患者可從治療中獲得更明顯的獲益(55.5%vs42.9%)。這提示,依達拉奉右莰醇在血管內治療前使用,可能通過減輕缺血再灌注損傷和繼發性炎癥而發揮“凍結半暗帶”的作用。急性缺血性卒中治療有望從單純依賴“時間窗”向更精準的“組織窗”評估的重要轉變。對于存在明顯“不匹配”的患者,積極采取聯合治療(腦細胞保護劑+再灌注治療)可能帶來顯著獲益。
“TASTE-2研究的結果非常令人鼓舞。”研究第一作者,北京天壇醫院王春娟教授表示:“它首次在嚴格設計的大樣本臨床試驗中證實,在取栓這一強大血流重建基礎上,加用多靶點腦保護藥物能夠進一步為患者帶來功能獲益。這不僅僅是藥物的成功,更代表了一種治療理念的落地——即‘血管再通’與‘腦細胞保護’協同并重的綜合治療模式,這可能成為未來卒中治療的新標準。”
依達拉奉右莰醇注射用濃溶液是先聲藥業有限公司自主研發的多靶點腦細胞保護劑,國家1類新藥。該藥物含依達拉奉和右莰醇兩種活性成分,可高效透過血腦屏障,通過抗炎和清除自由基雙效協同,減少腦缺血引發的級聯損傷。作為全球卒中治療領域自2015年以來唯一獲批上市銷售的創新藥,該藥物歷時12年研發,并兩次獲得國家“重大新藥創制”專項支持。
北京天壇醫院王擁軍教授團隊主導的TASTE研究,以及北京大學第三醫院樊東升教授牽頭的TASTE-SL研究,分別證實了依達拉奉右莰醇注射劑型,以及舌下片劑型對非取栓AIS患者的療效。相關數據于2021年和2024年發表在國際神經病學頂級期刊STROKE(《卒中》)和JAMA Neurology(《美國醫學會神經病學雜志》),為醫學界重啟了卒中腦細胞保護研究的大門。依達拉奉右莰醇舌下片也獲美國食品藥品監督管理局(FDA)突破性療法認定,是全球卒中治療領域首個被FDA認定為突破性療法的創新藥。
TASTE-2研究,證實了AIS患者在取栓前使用依達拉奉右莰醇可進一步獲益,以新的臨床證據不斷拓展著科學對“腦細胞保護”的認知。BMJ雜志的高級別臨床證據發表,有望推動腦細胞保護相關藥物作為取栓等血管內治療的聯合用藥,為進一步提升卒中治療效果,減少卒中致殘。(木子)
《中國醫藥報》社版權所有,未經許可不得轉載使用。
(責任編輯:郭肖)
右鍵點擊另存二維碼!
-
相關閱讀
-
為你推薦